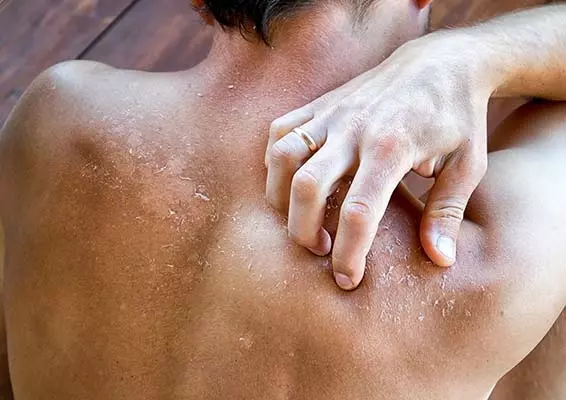
Atopowe zapalenie skóry to przewlekła choroba zapalna skóry charakteryzująca się okresami nawrotów i remisji. Jest najczęstszą dermatozą wieku dziecięcego, dotykającą prawie 20% populacji pediatrycznej. W grupie dorosłych częstość występowania AZS szacuje się na poziomie 2–10% [1].
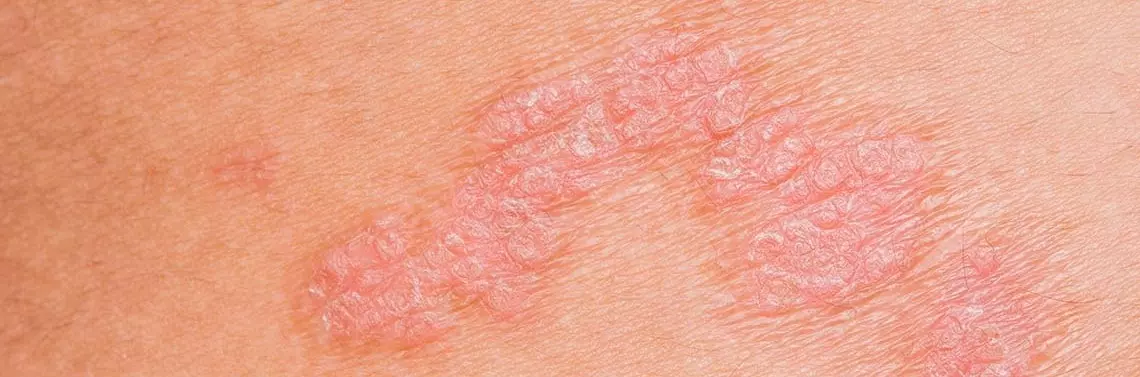
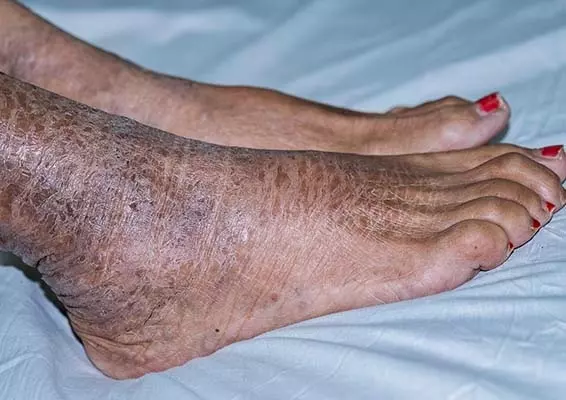
Na rozwój atopowego zapalenia skóry ma wpływ wiele czynników. Należą do nich: czynniki genetyczne, czynniki środowiskowe, nieprawidłowe funkcjonowanie bariery naskórkowej, zaburzenia immunologiczne oraz zakłócenie równowagi mikrobiologicznej. Najbardziej charakterystycznym objawem choroby jest uporczywy świąd oraz wykwity skórne o charakterze wyprysku pojawiające się w typowych dla wieku lokalizacjach. Atopowe zapalenie skóry wiąże się ze znacznym pogorszeniem jakości życia pacjentów, wpływając negatywnie na jakość snu, koncentrację, relacje towarzyskie. W przebiegu AZS obserwuje się zaburzenia depresyjne oraz lękowe [2].
Leczenie ogólne atopowego zapalenia skóry jest zarezerwowane dla pacjentów, u których przebieg choroby jest umiarkowany lub ciężki, a leczenie miejscowe nie przynosi zadowalających rezultatów i nie zapewnia kontroli objawów.
Do niedawna wachlarz opcji terapeutycznych pozostawał ograniczony, zwłaszcza w grupie pediatrycznej, a zastosowanie części leków, choć skutecznych, wiązało się z działaniami niepożądanymi przy ich długotrwałym przyjmowaniu. Do dyspozycji w leczeniu AZS o ciężkim przebiegu do tej pory zalecane były: systemowe kortykosteroidy (krótkie pulsy), cyklosporyna A, metotreksat, azatiopryna oraz mykofenolan mofetylu. Wśród tych leków jedynie cyklosporyna A jest zarejestrowana do leczenia dorosłych z ciężką postacią AZS. Kortykosteroidy systemowe są stosowane we wszystkich rekomendacjach, podkreśla się jednak zalecenie ich krótkoterminowego stosowania. Pozostałe leki stanowią grupę off-label w leczeniu AZS. Zatem leczenie postaci umiarkowanej i ciężkiej AZS stanowiło dotychczas wyzwanie.
Ostatnie lata obfitowały w wiele badań klinicznych nad lekami, które skupiają się na hamowaniu składowych układu immunologicznego, bezpośrednio lub pośrednio zaangażowanych w procesy leżące u podłoża reakcji zapalnej w atopowym zapaleniu skóry. W ten sposób pojawiły się dwie nowe strategie terapeutyczne w leczeniu ogólnym: przeciwciała monoklonalne skierowane przeciwko interleukinom lub ich receptorom oraz leki drobnocząsteczkowe hamujące szlaki sygnałowe JAK-STAT.
POLECAMY
Leki z grupy przeciwciał monok
...
Dołącz do grona specjalistów, którzy stale pogłębiają swoją wiedzę
Co trzy miesiące otrzymuj sprawdzone narzędzie i artykuły tworzone przez ekspertów-praktyków. Pogłębiaj wiedzę, pracuj sprawniej i bądź przygotowany na najbardziej skomplikowane przypadki.