Niealkoholowa stłuszczeniowa choroba wątroby
Niealkoholowa stłuszczeniowa choroba wątroby jest najczęstszą z chorób wątroby występującą na świecie i dotyczącą aż 30% populacji osób dorosłych w krajach rozwiniętych [1]. Prognozuje się, że NAFLD do 2030 r. będzie pierwszą przyczyną wykonywania przeszczepów wątroby w Stanach Zjednoczonych [2]. Niealkoholowa stłuszczeniowa choroba wątroby jest związana z występowaniem stłuszczenia w obrębie wątroby potwierdzonego badaniami obrazowymi lub badaniem histopatologicznym przy braku wtórnych przyczyn gromadzenia się tłuszczu w wątrobie (tab. 1), jak spożywanie nadmiernych ilości alkoholu, przyjmowanie niektórych leków czy choroby uwarunkowane genetycznie.
Do najważniejszych przyczyn rozwoju NAFLD należą otyłość, cukrzyca i dyslipidemia będące składowymi zespołu metabolicznego (tab. 2). Wśród czynników ryzyka niealkoholowej stłuszczeniowej choroby wątroby wymienia się także płeć męską, zespół policystycznych jajników, niedoczynność tarczycy, przysadki, obturacyjny bezdech senny, hipogonadyzm oraz resekcję trzustki i dwunastnicy.
Na podstawie obrazu histopatologicznego NAFLD dzieli się na:
POLECAMY
- niealkoholowe stłuszczenie wątroby (non-alcoholic fatty liver – NAFL) będące stłuszczeniem wątroby bez cech uszkodzenia hepatocytów. Progresja choroby jest powolna i rokowanie jest pomyślne,
- niealkoholowe stłuszczeniowe zapalenie wątroby (non-alcoholic steatohepatitis – NASH), w przebiegu którego obserwuje się współwystępowanie cech stłuszczenia i zapalenia wątroby ze zwyrodnieniem balonowatym hepatocytów z obecnym włóknieniem lub jego brakiem. Choroba ta może prowadzić do marskości wątroby. Notuje się zwiększoną umieralność w tej grupie pacjentów z powodu niewydolności wątroby [3].
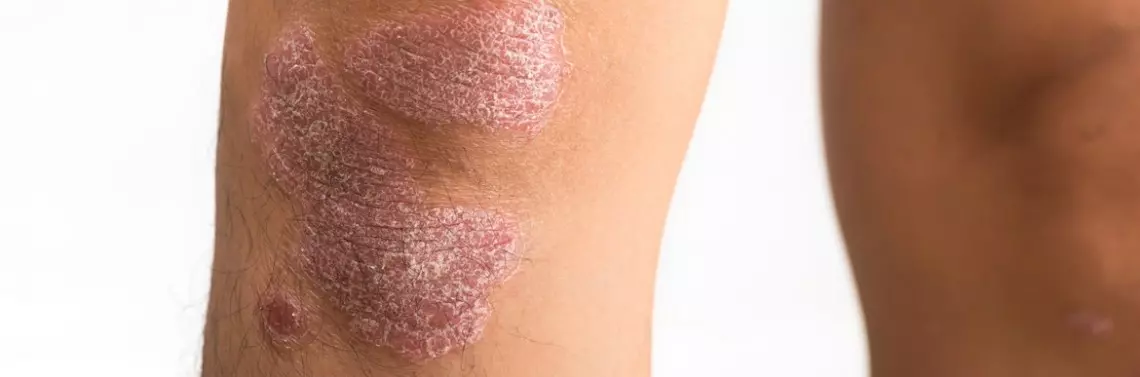
Łuszczyca
Łuszczyca jest przewlekłą, nawrotową, zapalną chorobą skóry, dotyczącą ok. 2–3% populacji światowej. Badania epidemiologiczne sugerują, że częstość łuszczycy zwiększa się w miarę oddalania od równika [4]. Wykwitem pierwotnym w łuszczycy jest rumieniowa grudka pokryta srebrzystą łuską, choć zmiany przybierają często postać większych tarczek lub plackowatych rumieniowych ognisk. Zmiany typowo lokalizują się na łokciach, kolanach, owłosionej skórze głowy oraz w okolicy krzyżowo-lędźwiowej, ale mogą zajmować każdą okolicę ciała oraz paznokcie. Około 1/3 pacjentów cierpi na postać stawową choroby, co w najpoważniejszych przypadkach może prowadzić nawet do inwalidztwa. W etiopatogenezie choroby biorą udział zarówno czynniki genetyczne, jak i środowiskowe. Wśród czynników genetycznych najsilniejsze powiązanie z łuszczycą ma ludzki układ zgodności tkankowej, kodowany przez geny zlokalizowane na chromosomie 6. W patogenezie choroby istotną rolę odgrywa dysregulacja dotycząca cytokin, prowadząca do wydzielania wielu prozapalnych mediatorów, co zwiększa proliferację keratynocytów. Łuszczyca uznawana jest za chorobę mediowaną przez limfocyty typu T, głównie Th 1 i Th 17, wytwarzające m.in. czynnik martwicy nowotworu alfa (tumor necrosis factor – TNF-α) oraz interleukinę (Il): 6, 17, 22 i interferon gamma (IFN-γ), co wpływa na nieprawidłowe różnicowanie i proliferację keratynocytów, rozszerzenie naczyń krwionośnych oraz infiltrację leukocytów do skóry [5]. Zidentyfikowano wiele czynników promujących powstawanie zmian skórnych w łuszczycy, takich jak miejscowe podrażnienie skóry (fenomen Koebnera), infekcje bakteryjne, stres, niektóre leki, jak IFN-α, sole litu czy beta-blokery oraz palenie papierosów [6]. Mimo że łuszczyca dotyczy przede wszystkim skóry, osoby cierpiące na tę chorobę są w większym stopniu narażone na rozwój chorób sercowo-naczyniowych, w związku z nasiloną aterogenezą, otyłości i zespołu metabolicznego oraz niealkoholowego stłuszczenia wątroby [7, 8].
Tab. 1. Przyczyny wtórnego stłuszczenia wątroby
| Stłuszczenie wielkokropelkowe |
nadmierne spożycie alkoholu, wirusowe zapalenie wątroby typu C, głodzenie, choroba Wilsona, żywienie pozajeli... |

Dołącz do grona specjalistów, którzy stale pogłębiają swoją wiedzę
Co trzy miesiące otrzymuj sprawdzone narzędzie i artykuły tworzone przez ekspertów-praktyków. Pogłębiaj wiedzę, pracuj sprawniej i bądź przygotowany na najbardziej skomplikowane przypadki.