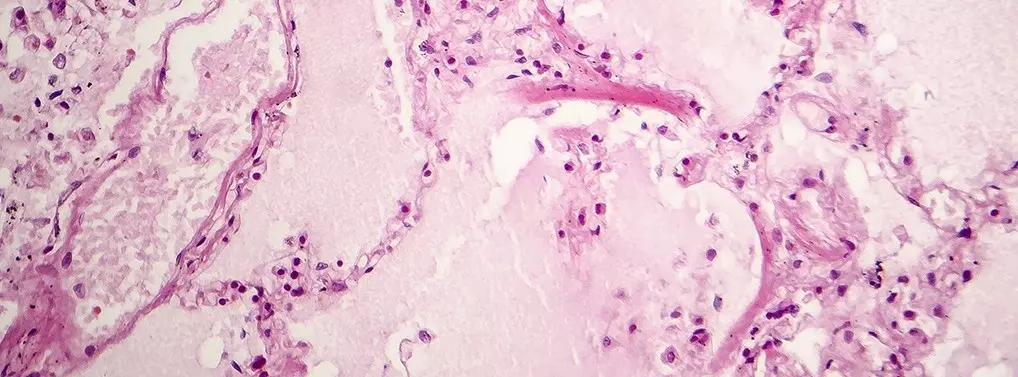
Obrzęk naczynioruchowy jest częstym objawem obserwowanym w gabinetach dermatologicznych i alergologicznych. Szacuje się, że wystąpi u 20–25% ogólnej populacji [1]. Jego przyczyny udaje się ustalić tylko w nieco ponad połowie przypadków [2]. Definiowany jest jako obrzęk tkanki podskórnej lub podśluzówkowej związany ze wzrostem przepuszczalności naczyń na skutek działania mediatorów naczynioaktywnych [3, 4]. Najczęściej mediatorem tym jest histamina, ale wczęści przypadków mogą to być inne mediatory, takie jak: bradykinina, prostaglandyna, leukotriany, czynnik aktywujący płytki (platelet-activating factor – PAF) i inne [3]. Właśnie bradykinina jest mediatorem naczynioaktywnym odgrywającym główną rolę w powstawaniu wrodzonego HAE [3, 5]. Jest to schorzenie rzadkie, bo występujące z częstością 1:50 000 w ogólnej populacji [6], ale ważne ze względu na możliwość zagrożenia życia w przypadku lokalizacji w obrębie górnych dróg oddechowych oraz braku reakcji na leczenie lekami antyhistaminowymi, glikokortykosteroidami, a nawet adrenaliną. W Polsce szacuje się, że choruje ok. 600–800 osób, jednak dotychczas zidentyfikowano nieco ponad 300 pacjentów, z czego wynika, że wielu pacjentów pozostaje nierozpoznanych i jest leczonych jak typowy obrzęk zależny od histaminy.
POLECAMY
Patofizjologia
Wrodzony obrzęk naczynioruchowy jest schorzeniem uwarunkowanym genetycznie, w większości przypadków spowodowanym mutacją w obrębie genu Serping 1 kodującego białko serpinę – C1-INH (inhibitor C1 składowej dopełniacza), należącego do kinaz białkowych. Zidentyfikowane mutacje powodują w przeważającej części przypadków niedobór tego białka, a w części przypadków niesprawność funkcjonalną. Wykryto także mutacje czynnika XII układu krzepnięcia, angiopoetyny 1 i plazminogenu [4, 7, 8]. Opisane zaburz...

Dołącz do grona specjalistów, którzy stale pogłębiają swoją wiedzę
Co trzy miesiące otrzymuj sprawdzone narzędzie i artykuły tworzone przez ekspertów-praktyków. Pogłębiaj wiedzę, pracuj sprawniej i bądź przygotowany na najbardziej skomplikowane przypadki.